Spektrofotometri adalah salah satu metode analisa yang didasarkan pada besarnya absorpsi suatu zat terhadap gelombang elektromagnetik. Singkatnya, Spektroskopi/ Spektrofotometri adalah metode kimia analisis untuk menentukan komposisi secara kuantitatif maupun kualitatif yang didasarkan pada interaksi antara materi dan cahaya.
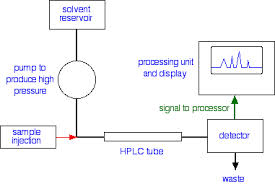
Spektrofotometer adalah alat untuk mengukur absorbansi dengan cara melewatkan cahaya dengan panjang gelombang tertentu pada suatu objek kaca/kuarsa (kuvet). Sebagian cahaya tsb akan diserap, dan sisanya akan dilewatkan. Prinsip kerja spektrofotometer ini merupakan gabungan prinsip dari spektrometer dan fotometer. Spektrometer sebagai penghasil sumber cahaya, dan fotometer sebagai pengukur intensitas cahaya yang diserap. Pada spektrometer terdapat alat pengurai seperti prisma yang dapat menyeleksi panjang gelombang dari sinar putih, dan pada fotometer terdapat filter. Spektrofotometer dilengkapi dengan sumber cahaya (gel. elektromagnetik) baik UV maupun Visible. Spektrofotometer mampu membaca dan mengukur kepekatan warna dari sampel tertentu dengan panjang gelombang tertentu.
Spektrofotometer :
1. Single Beam, cahaya hanya melewati 1 arah shg nilai yang diperoleh hanya nilai Absorabansi dari larutan yang dimasukkan.
2. Double Beam, nilai blanko dapat langsung diukur bersamaan dgn larutan yang diinginkan dalam 1 kali proses yang sama.
Sumber cahaya (polikromatis) → Monokromator → Sampel → Detektor → Read Out
Sumber radiasi :
UV: Deuterium/ Heavy Hydrogen (isotop)
Visible : Tungsten / wolfram
UV–Vis : Photodiode lengkap dengan monokromator
IR : lampu dengan panjang gelombang
Monokromator : Penyeleksi panjang gelombang. Untuk mengubah cahaya yang berasal dari sumber polikromatis menjadi cahaya monokromatis.
Jenis-jenis Spektrofotometri
Spektrofotometri terdiri dari beberapa jenis berdasarkan sumber cahaya yang digunakan. Diantaranya adalah sebagai berikut :
1) Spektrofotometri Vis (Visible)
Pada spektrofotometri ini yang digunakan sebagai sumber sinar/energi adalah cahaya tampak (Visible). Cahaya visible termasuk spektrum elektromagnetik yang dapat ditangkap oleh mata manusia. Panjang gelombang sinar tampak adalah 380-750 nm. Sehingga semua sinar yang dapat dilihat oleh mata manusia, maka sinar tersebut termasuk kedalam sinar tampak (Visible).
2) Spektrofotometri UV (Ultra Violet)
Berbeda dengan spektrofotometri Visible, pada spektrofometri UV berdasarkan interaksi sampel dengan sinar UV. Sinar UV memiliki panjang gelombang 190-380 nm. Karena sinar UV tidak dapat dideteksi oleh mata manusia maka senyawa yang dapat menyerap sinar ini terkadang merupakan senyawa yang tidak memiliki warna. Bening dan transparan.
3) Spektrofotometri UV-Vis
Spektrofotometri ini merupakan gabungan antara spektrofotometri UV dan Visible. Menggunakan dua buah sumber cahaya berbeda, sumber cahaya UV dan sumber cahaya visible. Meskipun untuk alat yang lebih canggih sudah menggunakan hanya satu sumber sinar sebagai sumber UV dan Vis, yaitu photodiode yang dilengkapi dengan monokromator.Untuk sistem spektrofotometri, UV-Vis paling banyak tersedia dan paling populer digunakan. Kemudahan metode ini adalah dapat digunakan baik untuk sampel berwarna juga untuk sampel tak berwarna. Spektrofotometri ultraviolet-visible (UV-Vis atau UV / Vis) melibatkan spektroskopi dari foton dalam daerah UV-terlihat. Ini berarti menggunakan cahaya dalam terlihat dan berdekatan (dekat ultraviolet (UV) dan dekat dengan inframerah (NIR)) kisaran. Penyerapan dalam rentang yang terlihat secara langsung mempengaruhi warna bahan kimia yang terlibat. Di wilayah ini dari spektrum elektromagnetik, molekul mengalami transisi elektronik. Teknik ini melengkapi fluoresensi spektroskopi, di fluoresensi berkaitan dengan transisi dari ground state ke excited state.
Penyerapan sinar UV dan sinar tampak oleh molekul, melalui 3 proses yaitu :
- Penyerapan oleh transisi elektron ikatan dan elektron anti ikatan.
- Penyerapan oleh transisi elektron d dan f dari molekul kompleks.
- Penyerapan oleh perpindahan muatan.
Interaksi antara energi cahaya dan molekul dapat digambarkan sbb :
E = hv
Dimana :
E = energy (joule/second)
h = tetapan planck
v = frekuensi foton
4) Spektrofotometri IR (Infra Red)
Spektrofotometri ini berdasar kepada penyerapan panjang gelombang Inframerah. Cahaya Inframerah, terbagi menjadi inframerah dekat, pertengahan dan jauh. Inframerah pada spektrofotometri adalah adalah inframerah jauh dan pertengahan yang mempunyai panjang gelombang 2.5-1000 mikrometer. Hasil analisa biasanya berupa signal kromatogram, hubungan intensitas IR terhadap panjang gelombang. Untuk identifikasi, signal sampel akan dibandingkan dengan signal standard. Kegunaannya u/ identifikasi senyawa organik krn spektrumnya sangat kompleks ( banyak puncak) dan sangat karakteristik.